Карбоновые кислоты | Конспект
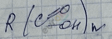
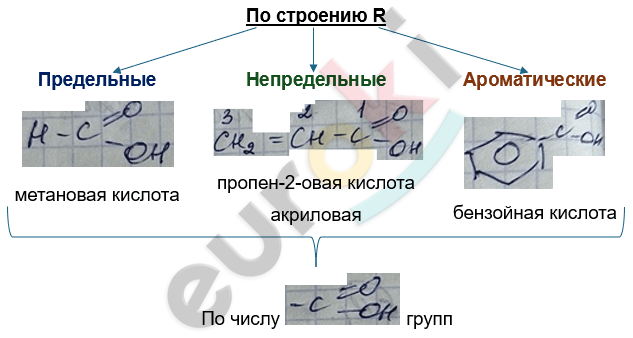
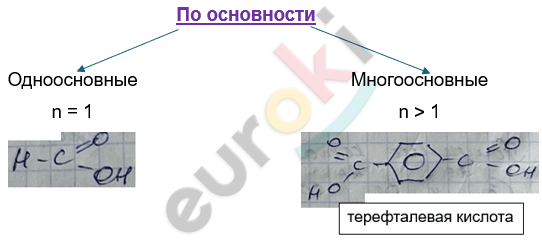
Изомерия одноосновных, предельных карбоновых кислот
1. С-скелета
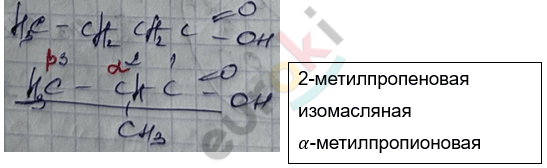
2. Межклассовая
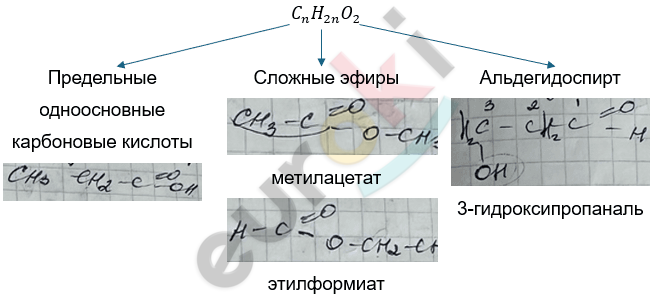
Низшие карбоновые кислоты \(С_{1} - С_{3}\) – жидкости, которые растворяются в воде, \(С_{4} - С_{10}\) – вязкотекучие жидкости, не растворяются в воде.
Высшие карбоновые кислоты (ВКК) с С более 10 – это твёрдые вещества, не растворимые в воде.
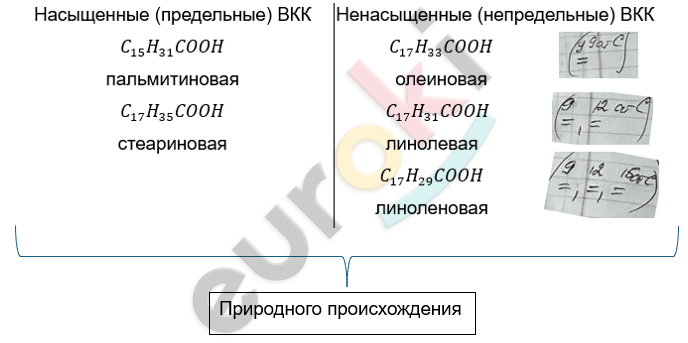

Химические свойства
1. Кислотные свойства
а) слабые электролиты

Фиолетовой лакмус становится красным.
Жёлто-оранжевый метилоранж становится розово-красным.
б) с металлом до водорода → соль + \(H_{2} \uparrow\)

в) с металлом х \(O_{y}\) → соль + \(H_{2}O\)

г) реакция с гидроксидами металлов (\({\text{Me}(\text{OH})}_{n}\))


Если используется не растворимое в воде основание, то такая реакция качественная, так как осадок растворяется с получением прозрачного раствора.
д) раствор с солями более слабых кислот:
- карбонаты, гидрокарбонаты;
- сульфиты;
- сульфиды;
- силикаты.
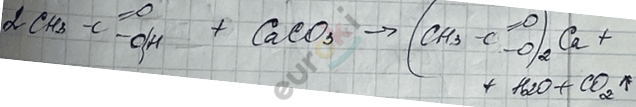
2. Реакция с \(\text{PCl}_{5}\), \(\text{PCl}_{3}\), \({\text{SO}\text{Cl}}_{2}\).
3. Реакция межмолекулярной реакции гидратации карбоновых кислот с получением их ангидридов.
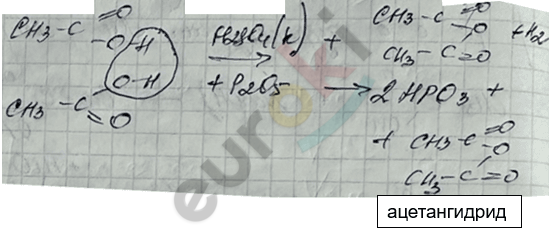
4. Реакция с \(\text{NH}_{3}\)
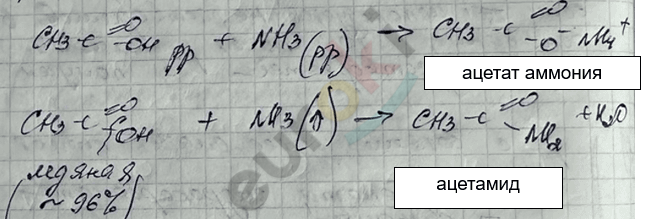
5. Реакция этерификации

6. Для предельных карбоновых кислот будет идти реакция замещения по \(\alpha\) С-атому
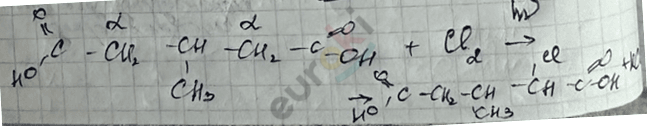
7. Все реакции по кратной связи радикала

8.